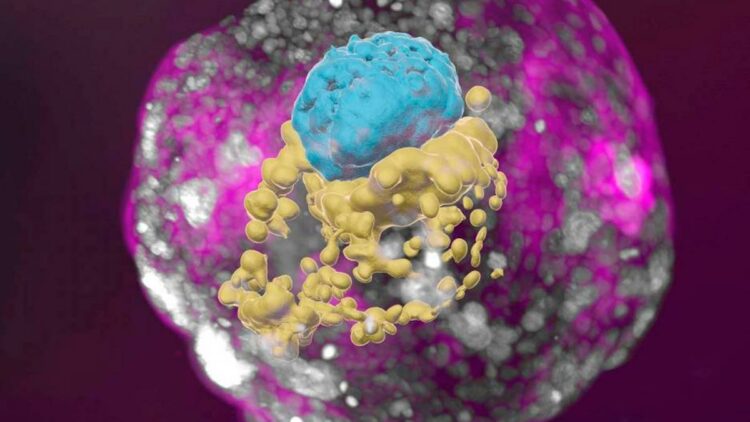
Un equipo de investigadores del Instituto Weizmann de Ciencias logró desarrollar modelos completos de embriones humanos a partir de células madre cultivadas en laboratorio, es decir, sin necesidad de óvulos ni esperma, y cultivarlos fuera del útero hasta el día 14, informó hoy el centro científico israelí.
«Los modelos de embriones sintéticos presentaban todas las estructuras y compartimentos característicos de esta etapa, incluyendo placenta, saco vitelino, saco coriónico y otros tejidos externos que aseguran el crecimiento dinámico y adecuado de los modelos», precisó hoy el Instituto Weizmann a través de un informe al que accedió Télam.
Este desarrollo es un gran avance de la ciencia, cuyo antecedente directo es un estudio de especialistas de la Universidad de Cambridge, Reino Unido, según el cual lograron el desarrollo de embriones sintéticos originados de células madre que «llegaron al inicio de una etapa crucial en el desarrollo conocida como gastrulación».
La investigación de ese momento se presentó en la reunión anual de la Internacional Society for Stem Cell Research, pero no fue publicada aún, ni revisada por otros científicos.
En este sentido, el centro de investigaciones científicas apuntaron que los «agregados celulares derivados de células madre humanas en estudios anteriores no podían considerarse modelos de embriones humanos genuinamente precisos, porque carecían de casi todas las características definitorias de un embrión postimplantación».
En particular, remarcó que «no contuvieron varios tipos de células que son esenciales para el desarrollo del embrión, como las que forman la placenta y el saco coriónico. Además, no tenían la organización estructural característica del embrión y no revelaban capacidad dinámica para avanzar a la siguiente etapa de desarrollo».
Dada su auténtica complejidad, los modelos de embriones humanos obtenidos por el grupo del Instituto, liderado por Jacob Hanna, abren la puerta a una oportunidad «sin precedentes para arrojar nueva luz sobre los misteriosos orígenes del embrión».
Desde la institución se destacó que la importancia del estudio radica en la escasa investigación que existe al respecto «tanto por razones éticas como técnicas» y remarcó que las etapas iniciales del trabajo «son cruciales para su desarrollo futuro», ya que son esos momentos en los que el conjunto de células que se implanta en el útero (al séptimo día de su existencia) se convierte, al cabo de tres o cuatro semanas, en un embrión bien estructurado que ya contiene todos los órganos del cuerpo.
«El drama ocurre en el primer mes, los ocho meses restantes del embarazo son principalmente de mucho crecimiento», dijo Hanna, y enfatizó en que «ese primer mes sigue siendo una caja negra».
«Nuestro modelo de embrión humano derivado de células madre ofrece una forma ética y accesible de mirar dentro de esta caja. Imita fielmente el desarrollo de un embrión humano real, en particular el surgimiento de su arquitectura exquisitamente fina», señaló el especialista.
Este estudio tomó como base su experiencia previa en la creación de modelos de embriones de ratón basados en células madre sintéticas sin óvulos fertilizados ni útero.
En esta ocasión «comenzaron con células humanas conocidas como células madre pluripotentes, que tienen el potencial de diferenciarse en muchos -aunque no todos- tipos de células».
Los investigadores utilizaron el método desarrollado recientemente por Hanna para reprogramar células madre pluripotentes con el objetivo de retroceder aún más el reloj: revertir estas células a un estado aún anterior, conocido como estado ingenuo, en el que son capaces de convertirse en cualquier cosa, es decir, especializándose en cualquier tipo de célula. Esta etapa corresponde al día 7 del embrión humano natural, aproximadamente el momento en que se implanta en el útero.
«Un embrión no es estático. Debe tener las células adecuadas en la organización adecuada y debe poder progresar porque se trata de ser y llegar a ser», dijo Hanna. «Nuestros modelos completos de embriones ayudarán a los investigadores a abordar las preguntas más básicas sobre qué determina su crecimiento adecuado». agregó.
«Este enfoque ético para descubrir los misterios de las primeras etapas del desarrollo embrionario podría abrir numerosos caminos de investigación y ayudar a revelar las causas de muchos defectos congénitos y tipos de infertilidad», explicaron desde el Instituto Weizmann.
Y agregaron que «también podría conducir a nuevas tecnologías para el cultivo de tejidos y órganos para trasplantes y ofrecer soluciones a experimentos que no es posible realizar con embriones vivos como determinar los efectos de la exposición a drogas u otras sustancias en el desarrollo fetal.
En 2013, el equipo de Hanna fue el primero en comenzar a describir métodos para generar células madre humanas vírgenes y desde ese momento continuó con investigaciones que profundizaron y mejoraron esos métodos, que son el núcleo del proyecto actual, a lo largo de los años.